научное издание МГТУ им. Н.Э. Баумана
НАУКА и ОБРАЗОВАНИЕ
Издатель ФГБОУ ВПО "МГТУ им. Н.Э. Баумана". Эл № ФС 77 - 48211. ISSN 1994-0408
# 01, январь 2014
DOI: 10.7463/0114.0681975
УДК: 536.75
| УДК 536.75 | Россия, МГТУ им. Н.Э. Баумана |
Разработка методов описания процессов, происходящих в неравновесных системах, требует применения новых подходов. Дело в том, что в отличие от процессов, происходящих в квазиравновесных системах, для которых применимы методы равновесной термодинамики, при описании сильно неравновесных систем возникает необходимость использования соотношений, отличающихся от обычно применяемых в линейной термодинамике [1, 2]. В частности, в качестве альтернативы линейным кинетическим соотношениям выступает применение интегральных преобразований, описывающих немарковские процессы [3].
Стремление энтропии к максимальному значению при приближении термодинамической системы к равновесному состоянию описывается разными функциями, в зависимости от степени неравновесности системы. Если система находится в близком к равновесию состоянии, то её стремление к максимальному значению происходит максимально быстро и описывается экспоненциальной зависимостью. Для далеких от равновесия состояний возрастание энтропии происходит максимально медленно и описывается логарифмической зависимостью. Покажем это на простом примере.
Пусть имеется термодинамическая система, состоящая из двух находящихся в тепловом контакте тел, помещенная в адиабатическую оболочку. Считаем, что тела имеют идеальную (бесконечно высокую) теплопроводность. Теплоемкости тел одинаковы и равны ![]() . Температура первого тела в некоторый момент времени равна
. Температура первого тела в некоторый момент времени равна ![]() , а второго -
, а второго - ![]() , причем
, причем ![]() . Найдем уравнение, описывающее изменение энтропии системы с течением времени при её стремлении к состоянию термодинамического равновесия. Будем считать, что передача теплоты от одного тела к другому описывается формулой
. Найдем уравнение, описывающее изменение энтропии системы с течением времени при её стремлении к состоянию термодинамического равновесия. Будем считать, что передача теплоты от одного тела к другому описывается формулой
| (1) |
где ![]() - коэффициент теплопередачи.
- коэффициент теплопередачи.
После достижения системой состояния термодинамического равновесия температура тел станет одинаковой
| (2) |
а её энтропия примет максимальное значение ![]() .
.
Изменение энтропии системы при её переходе в равновесие можно определить по формуле
 | (3) |
Из этой формулы следует
 | (4) |
В соответствии со свойством аддитивности энтропии для изменения энтропии рассматриваемой системы можно записать
 | (5) |
Здесь учтено, что теплота отводится от второго тела и подводится к первому.
Тогда уравнение, описывающее изменение энтропии с течением времени при стремлении системы к состоянию термодинамического равновесия, примет окончательный вид
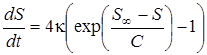 | (6) |
При ![]() правая часть этого уравнения больше нуля, что соответствует росту энтропии с течением времени:
правая часть этого уравнения больше нуля, что соответствует росту энтропии с течением времени: ![]() . При достижении энтропией системы
. При достижении энтропией системы ![]() равновесного (максимального) значения
равновесного (максимального) значения ![]() , правая часть полученного уравнения становится равной нулю, и дальнейшего роста энтропии не происходит.
, правая часть полученного уравнения становится равной нулю, и дальнейшего роста энтропии не происходит.
Если считать, что в начальный момент времени энтропия ![]() , то решение уравнения (6) можно записать в неявном виде [4]
, то решение уравнения (6) можно записать в неявном виде [4]
 | (7) |
Получим решение для двух частных случаев. В первом будем считать, что термодинамическая система находится в состоянии, близком к равновесному: ![]() . Тогда, приближенное решение уравнения (6), имеет вид
. Тогда, приближенное решение уравнения (6), имеет вид
 | (8) |
Из выражения (8) следует, что в состояниях, близких к равновесному, энтропия экспоненциально стремится к своему максимальному значению.
Рассмотрим теперь случай, когда термодинамическая система находится в состоянии, далеком от равновесия: ![]() . Решение (6) в этом случае имеет вид:
. Решение (6) в этом случае имеет вид:
 | (9) |
Как следует из выражения (9), в состояниях далеких от равновесия энтропия стремиться к максимальному значению по логарифмическому закону. Хотя логарифмическая функция и является более пологой, чем экспоненциальная, скорость увеличения энтропии, рассчитанная по формуле (9) оказывается имеющей большую величину, чем в случае применения формулы (8).
Результат численного решения уравнения (6) приведен на рис. 1 (средняя кривая 2) при следующих значениях параметров: ![]() ,
, ![]() ,
, ![]() и
и ![]() . На этом же рисунки приведены кривые, рассчитанные по формуле (8) (нижняя кривая 3) и по формуле (9) (верхняя кривая 1). Видно, что решение (8), соответствующее случаю описания термодинамической системы в состоянии близком к равновесию, достаточно явно не совпадает с численным решением уравнения (6) при сильно неравновесном состоянии. Результат, полученный по формуле (9), расходится с численным моделированием в области, близкой к равновесию.
. На этом же рисунки приведены кривые, рассчитанные по формуле (8) (нижняя кривая 3) и по формуле (9) (верхняя кривая 1). Видно, что решение (8), соответствующее случаю описания термодинамической системы в состоянии близком к равновесию, достаточно явно не совпадает с численным решением уравнения (6) при сильно неравновесном состоянии. Результат, полученный по формуле (9), расходится с численным моделированием в области, близкой к равновесию.
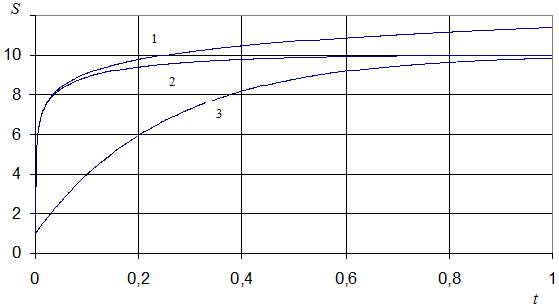
Рис. 1. Зависимость энтропии от времени: 1 – при описании с помощью
формулы (9), 2 - при решении уравнения (6), 3 – при описании с помощью
формулы (8)
Таким образом, рассмотренный простой пример показывает, что характер стремления энтропии к максимальному значению различен для систем, находящихся в состоянии близком к равновесию и для сильно неравновесных состояний. Полученные зависимости сохраняют свой вид и при описании необратимых процессов в более сложных термодинамических системах и, видимо, имеют достаточно универсальный характер.
Список литературы
- Леонтович М.А. Введение в термодинамику. Статистическая физика. М.: Наука, 1983. 416 с.
- Глаголев К.В., Морозов А.Н. Физическая термодинамика. М.: Изд-во МГТУ им. Н.Э. Баумана, 2007. 272 с.
- Morozov A.N., Skripkin A.V. Spherical particle Brownian motion in viscous medium as non-Markovian random process // Physics Letters A. 2011. Vol. 375, no. 46. P. 4113-4115. DOI: 10.1016/j.physleta.2011.10.001
- Прудников А.П., Брычков Ю.А., Маричев О.И. Интегралы и ряды. М.: Наука, 1981. 800 с.
Публикации с ключевыми словами: энтропия, термодинамическая система, неравновесное состояние, необратимый процесс
Публикации со словами: энтропия, термодинамическая система, неравновесное состояние, необратимый процесс
Смотри также:
Тематические рубрики:
| Авторы |
| Пресс-релизы |
| Библиотека |
| Конференции |
| Выставки |
| О проекте |
| Телефон: +7 (915) 336-07-65 (строго: среда; пятница c 11-00 до 17-00) |
|
||||
| © 2003-2024 «Наука и образование» Перепечатка материалов журнала без согласования с редакцией запрещена Тел.: +7 (915) 336-07-65 (строго: среда; пятница c 11-00 до 17-00) | |||||



